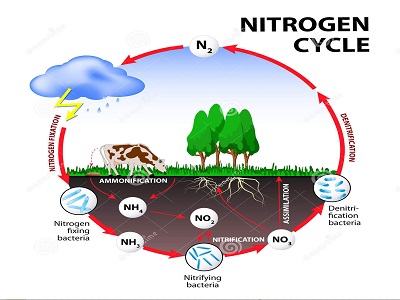
ALTRE FORME DI NITRIFICAZIONE E DENITRIFICAZIONE
Esistono poi altre forme di nitrificazione/denitrificazione di cui si è venuti solo recentemente a conoscenza: AOA (Ammonia-Oxidizing Archaea); DNRA (Dissimilatory Nitrate/nitrite Reduction to Ammonium); ANAMMOX (ANaerobic AMMonium OXidation)
AOA – Archeobatteri che ossidano l’ammonio (nitrificanti)
Il nome di questi microrganismi fa riferimento alla loro antica origine. Questi batteri sono in grado di vivere in ambienti estremi dove la sopravvivenza è difficile per molte forme di vita. L’ambiente in cui vivono è probabilmente molto simile a quello presente sulla terra durante le prime fasi di sviluppo dei procarioti.
Sono costituiti da singole cellule mancanti di nucleo e assieme ai batteri sono stati classificati come procarioti. Tuttavia questa classificazione è stata più volte rimaneggiata ed è tutt’ora oggetto di studio.
Esistono sottogruppi di questi batteri che vivono in condizioni di estrema salinità dell’acqua (alofili), oppure in habitat molto acidi e molto caldi (60-80°C e pH 2-4) e vengono denominati termoacidofili, oppure vi sono i metanogeni che producono metano in condizioni di totale mancanza di ossigeno.
Nonostante gli ambienti estremi in cui riescono a vivere, gli archeobatteri sono presenti anche in ambienti più ospitali.Gli archeobatteri si distinguono quindi dagli eubatteri che sono invece definiti come un sottoregno dei bacteria (ovvero i batteri).
Le profonde differenze evolutive che dividono gli eubatteri dagli archeobatteri non erano evidenti sulla base del fenotipo, mentre divenne chiaro solo dopo il confronto delle loro sequenze nucleotidiche. L’ipotesi che esistano tre gruppi evolutivi principali in seno agli organismi è confortata anche dalle sequenze di altri geni come quelle dei geni per alcune proteine di base, per alcuni RNA ribosomiali. Questi tre gruppi sono Crenarchaeota, Euryarchaeota e Korarchaeota.
Gli archea sono in grado di: ossidare l’ammonio a nitrito senza che vi sia il normale passaggio attraverso l’idrossilamina; possono sopportare la disidratazione, tanto da vivere in acque satura di sale (Halobacterium); sono stati trovati sui fondali oceanici vicino a bocche eruttive a temperature di 120° ed oltre e a pressioni elevatissime che impediscono l’ebollizione dell’acqua; la loro parete è priva di peptidoglicani, catene lineari di polisaccaridi che costituiscono le pareti cellulari degli Eubatteri; le loro membrane cellulari sono costituite da catene di isoprene e non da fosfolipidi; possiedono un pigmento sensibile alla luce rossa, la alorodopsina (molto simile alla rodopsina, presente anche nella retina dei Vertebrati) che serve loro per ottenere energia.
DNRA – Riduzione anaerobica dei nitrati ad ammonio (denitrificanti)
Molto spesso ci si riferisce al processo di denitrificazione come ad una sequenza di reazioni che, partendo dai nitrati, passando dai nitriti ed arrivando ad ammonio porti successivamente alla liberazione di azoto gassoso: NO3– —> NO2– —> NH4+ —> N2
Questa ovviamente è una semplificazione, o meglio una sintesi di due importanti meccanismi di denitrificazione che si servono di distinti batteri ed enzimi per arrivare a quell’obiettivo: la denitrificazione vera e la DNRA.
Denitrificazione vera (dissimilativa):
NO3− —> NO2− —> 2NO2– —> N2O —> N2DNRA
NO3− —> NO2− —> NH4+
Queste avvengono in condizioni simili di basse concentrazioni di ossigeno, ma mentre la denitrificazione dissimilativa trasforma il nitrato in nitrito, da qui in ossido nitrico e passando per l’ossido nitroso, arriva ad azoto gassoso, senza passare per l’ammoniaca, nella DNRA il passaggio da nitrato prevede dapprima la trasformazione in nitrito e poi subito in ammoniaca. Qui la reazione mediata da questi batteri si interrompe. Questo processo viene anche definito ammonificazione fermentativa.
 L’importanza della DNRA sta nel fatto che il nitrato viene convertito in una diversa forma minerale di azoto che è meno mobile e, sebbene sia in contrasto con la denitrificazione, essa è in grado di conservare l’azoto nell’ecosistema senza disperderlo nell’atmosfera sotto forma di gas.
L’importanza della DNRA sta nel fatto che il nitrato viene convertito in una diversa forma minerale di azoto che è meno mobile e, sebbene sia in contrasto con la denitrificazione, essa è in grado di conservare l’azoto nell’ecosistema senza disperderlo nell’atmosfera sotto forma di gas.
Per questo motivo la DNRA è stata definita come un cortocircuito nel ciclo biologico dell’azoto, in quanto il diretto trasferimento del nitrato in nitrito e poi ammoniaca bypassa la denitrificazione e la fissazione.
Le due reazioni della DNRA sono catalizzate da due enzimi di cui uno, il primo (da nitrato a nitrito) è respiratorio, mentre il secondo (da nitrito ad ammoniaca) è fermentativo.
La DNRA è stata ampiamente studiata in contesti acquatici (in particolare negli ecosistemi marini), mentre non ci sono ancora studi approfonditi su questo processo quando avviene nel suolo.
La presenza delle radici nel suolo modifica la denitrificazione come conseguenza dell’alterazione del substrato e della disponibilità di ossigeno ed è quindi ormai assodato che la denitrificazione è stimolata dalla presenza di radici. Ma questi dati sono disponibili solo per ambienti umidi e per piante acquatiche.
Uno studio in tal senso ha evidenziato come in un vaso piantumato l’attività della DNRA fosse del 53% contro un 71% a vantaggio della denitrificazione che si verifica in un terreno non piantumato. Tuttavia il contributo delle radici al processo DNRA nel suolo si è attestato essere solo dell’1% in più rispetto allo stesso terreno non piantumato.
Un altro studio condotto su zone acquitrinose in periodo di riposo vegetale, la DNRA predominava sulla denitrificazione.
Una ritenzione di azoto significativa è stato ottenuta in uno studio in cui la DNRA avveniva in terreni piantumati di suoli montagnosi tropicali.Oltre l’assimilazione da parte della pianta, la ritenzione di azoto nel terreno può essere dovuta all’assorbimento di ammoniaca prodotta tramite processo DNRA su terreni argillosi (in ragione della opposta carica elettrica) o sostanze organiche.
Sebbene il processo DNRA non preveda l’intermedio dell’ossido nitroso (N2O) tipico della denitrificazione, sono stati scoperti ceppi batterici (non ancora identificati precisamente) capaci di tale reazione. Gli studiosi suggeriscono che questo sistema rappresenti un meccanismo di detossificazione per evitare alte concentrazioni di nitrito.
L’impegno detossificante in un batterio con metabolismo DNRA non supera comunque l’1% della riduzione da nitrito a nitrato.Da studi condotti sono stati evidenziati diversi generi di batteri capaci di processi DNRA:
– Clostridium
– Citrobacter
– Enterobacter
– Erwinia
– Escherichia
– Klebsiella
– Bacillus
– Pseudomonas
– Arthrobacter
ANAMMOX – Ossidazione anaerobica dell’ammonio (denitrificanti)
La reazione anammox è importante in quanto fino a qualche anno fa non si erano ancora individuati ceppi batterici capaci di metabolizzare l’ammonio in condizioni anaerobiche. Pertanto si credeva che l’ammonio nei sedimenti dei bacini idrici giacesse immodificato ed inerte.
Nel 2008 vennero isolati per la prima volta dei batteri marini appartenenti al genere Scalindua. Dopo di allora molti altri sono stati individuati ed appartengono all’ordine dei Planctomycetesdi tra cui Planctomyces e Pirellula sono i generi più noti.
Altri generi sono al vaglio: Brocadia, Kuenenia, Anammoxoglobus, Jettenia (tutti di acqua dolce) e Scalindua (di acqua marina).
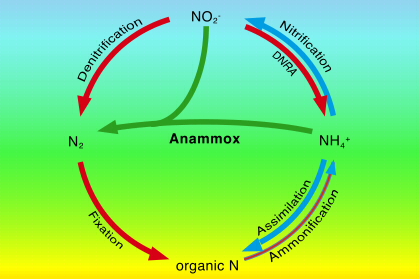
L’ammonio è ossidato ad azoto molecolare usando il nitrito come accettore di elettroni. La reazione è la seguente: NH4+ + NO2– –> N2 + 2H2O
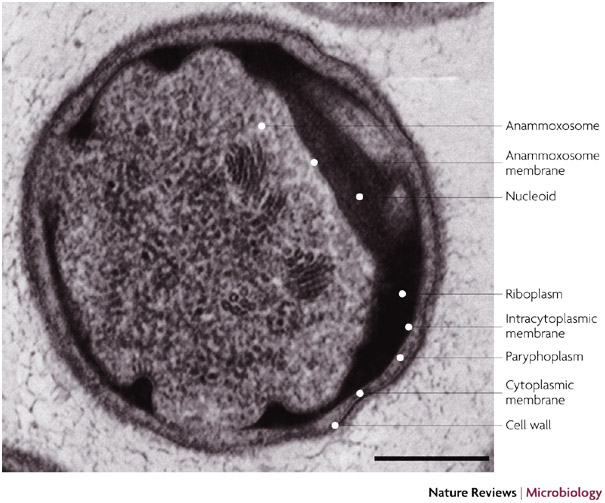
Questa reazione batterica avviene nell’anammoxosoma che è un compartimento intracitoplasmatico racchiuso da una membrana a singolo stato lipidico.
Tale struttura appare inusuale, dato che rappresenta un organello che è più tipicamente presente negli organismi eucarioti.
Il processo Anammox è strettamente autotrofo e anaerobico e prevede l’idrossilamina come intermedio di passaggio. L’ammonio con idrossilamina è convertito ad idrazina e successivamente questa è ossidata ad azoto bimolecolare.
La presenza della membrana dell’anammoxosoma ha anche il significato di isolare dal resto della cellula l’idrazina in quanto sostanza altamente reattiva.
L’importanza delle reazioni anammox risultano evidenti quando accostate a quelle del processo DNRA sopradescritto, infatti se poste in sequenza DNRA —> Anammox si realizza una completa ossidazione da nitrato ad azoto molecolare in condizioni del tutto anaerobiche.
Da studi condotti pare che il contributo complessivo della reazione anammox negli oceani alla produzione di azoto gassoso sia del 50% nei confronti di tutto l’azoto prodotto e liberato nell’atmosfera.
5) VOLATILIZZAZIONE
Perdite di azoto ammoniacale si possono verificare per evaporazione in una soluzione in cui vi sia dell’ammoniaca. Vediamo come.
Gli ioni ammonio (NH4+) sono principalmente molecole di ammoniaca anidra (NH3+) a cui legato uno ione idrogeno (H+). Quando uno ione idrogeno viene rimosso da una molecola di ammonio da un altro ione idrossile (OH–), la molecola risultante di ammoniaca può evaporare o volatilizzarsi.
Questo fenomeno è maggiormente presente in soluzioni ad alto pH che contengano grandi quantità di ioni idrossile (OH–).
Perchè nel terreno la volatilizzazione possa avere luogo è necessario che siano presenti ioni ammonio in soluzione, in quanto la reazione non si applica agli ioni ammonio adsorbiti dalla capacità di scambio cationico del terreno (per effetto dell’attrazione di cariche opposte).
La velocità della volatilizzazione dell’ammoniaca dipende dalla temperatura e dalle condizioni del vento, all’aumentare delle quali l’equilibrio tra ammonio e ammoniaca (NH4+ <—> NH3 + H+) si sposta verso la formazione di ammoniaca (a destra nella formula), provocando un aumento della costante di volatilizzazione.
Continua