Il pH è definibile come la concentrazione degli ioni H+ (dal latino pondus Hydrogenii: peso degli ioni idrogeno) di una soluzione ed è espressa su base logaritmica negativa.
Questo significa che la variazione di un punto sulla scala del pH corrisponde ad una variazione di 10 volte la concentrazione degli ioni H+.
Come esiste un pH esiste anche un pOH che è definito come il logaritmo negativo della concentrazione degli ioni OH–. La somma del pH e del pOH deve essere sempre uguale a 14. L’acqua ha la formula chimica di H2O. Tuttavia essa non rimane necessariamente tale ma può subire una dissociazione.
Due molecole di acqua possono reagire secondo la seguente reazione:
2H2O —> H3O+ + OH–
oppure, per semplificare:
H2O —> H+ + OH–
Questo processo, definito auto dissociazione dell’acqua, interessa in realtà una quantità molto bassa di molecole di acqua.
Nell’acqua distillata la concentrazione di H+ e di OH– sono uguali, pertanto è da considerarsi chimicamente neutra. L’acqua assolutamente pura è quindi neutra. L’acqua neutra per convenzione viene definita al valore 7,0 di pH.
Variazioni dalla neutralità possono avvenire al di sotto di tale valore, per cui la soluzione viene definita acida, oppure al di sopra di tale valore, e la soluzione viene definita alcalina.
Il pH solitamente assume valori che vanno da 0 a 14, ma in alcuni casi particolari possono presentarsi valori molto distanti da questo intervallo (è il caso di soluzioni acide o basiche altamente concentrate).
Se l’acqua contiene sostanze acide, cioè sostanze in grado di rilasciare ioni H+ in soluzione, la loro concentrazione aumenterà ed il pH della soluzione si abbasserà.
COSA FA VARIARE IL PH NEL LAGHETTO
L’anidride carbonica (CO2) del laghetto ed il pH sono influenzati dalla respirazione batterica (meccanismo col quale una cellula batterica, in presenza di ossigeno, è in grado di ottenere energia per il proprio sostentamento) e dalla fotosintesi clorofilliana (che è un processo chimico grazie al quale le piante verdi producono sostanze organiche, principalmente carboidrati, a partire dall’anidride carbonica atmosferica e dall’acqua). 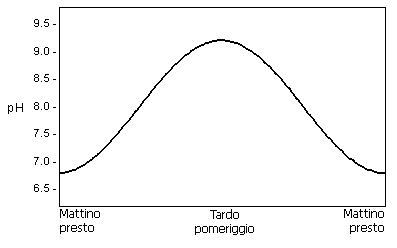
L’anidride carbonica è prodotta dalla respirazione e viene consumata dalla fotosintesi.Come effetto di questo, il pH subisce delle variazioni circadiane (cioè che avvengono nell’arco dell’intera giornata).
Le piante del laghetto e le alghe, eventualmente presenti, assorbono CO2 per produrre zucchero. A mano a mano che la luce del giorno si intensifica, la velocità della fotosintesi aumenta pertanto aumenta anche la velocità di assunzione della CO2.
La sottrazione di CO2 dall’acqua del laghetto, riduce la concentrazione di acido carbonico ed il pH del laghetto si alza.
Infatti in acqua la CO2 reagisce formando acido carbonico (H2CO3) e questo si dissocia in ione idrogeno (H+) e carbonato (HCO3–) secondo la formula: CO2 + H2O <—> H2CO3 <—> H+ + HCO3–
Il carbonato ed il bicarbonato sono due molecole che derivano dallo scioglimento del calcare presente nell’acqua. Sono responsabili della proprietà dell’acqua chiamata alcalinità che è la capacità dell’acqua di neutralizzare gli acidi.
Le interazioni chimiche tra anidride carbonica, ioni idrogeno e bicarbonato costituiscono la riserva alcalina che è un grado di mantenere il pH del nostro laghetto entro valori compresi tra 6,0 e 8,5 (vedi KH).
In assenza di processi che aggiungono o rimuovono l’anidride carbonica, il valore del pH del laghetto in contatto con l’aria dipende inizialmente dalla sua alcalinità. Maggiore è l’alcalinità dell’acqua e maggiore risulterà il suo pH. Aggiunta o rimozione di anidride carbonica dall’acqua modifica il pH.
L’estensione della variazione di pH dipenderà quindi dalla concentrazione di anidrice carbonica e dalla quantità di alcalinità dell’acqua.La respirazione batterica è influenzata dalla temperatura dalla biomassa delle piante, dai pesci, dai microrganismi dell’acqua e dai sedimenti presenti sul fondo del laghetto.
La velocità della fotosintesi è influenzata principalmente dall’intensità della luce solare, la biomasssa stessa delle piante e dalla temperatura. Durante la stagione calda, l’alta concentrazione di nutrienti nel laghetto, prodotta da scarti di alimentazione dei pesci, che a quelle temperature hanno un metabolismo molto rapido, può dare inizio ad una esplosione algale che è responsabile della sottrazione di CO2 dall’acqua in quantità significativa.
Dopo il tramonto, la quota di CO2 sottratta all’acqua dalla fotosintesi, termina, mentre la respirazione batterica continua ininterrotta. Questo determina un accumulo di CO2 nell’acqua che fa abbassare i valri del pH raggiungendo i valori più bassi 1-2 ore prima dell’alba. La variazione di pH è dannosa per le koi soprattutto in presenza di ammoniaca (NH4+) in quanto essa è presente nell’acqua in un’altra forma, l’ammonio (NH3) che è in equilibrio con l’ammoniaca secondo la formula: NH4+ + OH- <—> NH3 + H2O
L’aumento del pH determina uno spostamento della reazione verso destra con produzione di ammoniaca, che tra le due è la forma più tossica.
Le Koi si trovano quindi a subire due tipi di stress, quello dovuto alla variazione di pH e quello dovuto alla tossicità dell’ammoniaca.
Per questo motivo non si dovrebbe alimentare le koi nelle tarde ore pomeridiane, in quanto l’abbassamento del pH delle ore notturne mantiene in ammoniaca la quota prodotta dai pesci, senza che questa possa trovare equilibrio detossificante nella sua forma innocua, cioè l’ammonio.La concentrazione del fitoplancton (alga unicellulare) nei laghetti si sviluppa secondo periodi di fioritura e periodi di quiescenza.
Quando una grande quantità di fitoplancton muore, i nutrienti rilasciati dalla loro decomposizione tornano in soluzione nell’acqua, stimolando una nuova fioritura algale.
Quando le piante crescono rapidamente in primavera il rapido assorbimento di CO2 causa aumenti nel pH fino a quando il fitoplancton raggiunge un nuovo equilibrio.
Estesi periodi di pH elevato sono frequenti nei laghetti nei quali le alghe filamentose dominano numericamente rispetto alle piante. I laghetti con le alghe filamentose generalmente presentano acqua chiara che permette ai raggi solari di penetrare meglio lo spessore di acqua e stimolare quindi la fotosintesi.Problemi col pH sembrano insorgere maggiormente in quei laghetti che presentino una durezza alcalina (KH: durezza carbonatica) eccede di molto la durezza totale dell’acqua (GH: durezza magnesica e calcica).
VALORI IDEALI PER LE KOI
Le koi hanno le loro migliori condizioni di pH nell intervallo tra 7,0 e 8,6, ma la cosa più importante del valore assoluto del pH è la sua stabilità nel tempo.
Per accertarsi che non vi siano oscillazioni pericolose, il pH va misurato diverse volte durante il giorno in modo da avere un quadro preciso della modifica circadiana.
Esistono test con reagenti, altri con lettura fotometrica, altri con lettura digitale e quest’ultimo risulta il più pratico e rapido da eseguire (basta immergere la sonda per alcuni secondi nell’acqua ed il display mostrerà il valore del pH).
SINTOMI DELLA VARIAZIONE DI PH
I sintomi della variazione del pH variano a seconda che essa insorga bruscamente o cronicamente (lentamente).
Variazioni improvvise
Una variazione improvvisa anche entro l’intervallo tollerato normalmente dal pesce produce quasi sempre la morte.
La suscettibilità alla variazione improvvisa aumenta se il pesce è piccolo ed è più alta negli avannotti.
Variazioni improvvise del pH verso l’acidità possono essere date da forti temporali che trasportano durante la precipitazione sostanze acide mescolate alle gocce di acqua. Gli acquazzoni primaverili ed estivi sono evenienze ancora più pericolose se il laghetto si trova in presenza di bassa riserva alcalina rappresentata dai bicarbonati (KH). Valori inferiori a 3-4° tedeschi mettono a serio rischio il laghetto che non è in grado di tamponare l’acidità con una adeguata quantità di sostanze alcaline.
Variazioni che insorgono e si mantengono nel tempo
Generalmente condizioni di alcalosi sono più frequenti rispetto alle condizioni di acidosi, specialmente in laghetti appena allestiti.
Se il ph è troppo alto (pH>9,0 condizione definita alcalosi) i sintomi sono:
• Anoressia (il pesce non mangia).
• Letargia, svogliatezza, lentezza di reazione.
• Eccesso di produzione di muco.
• Isolamento.
• Scoloramento o variazione dei colori della koi.
• Screpolatura della pelle.
• Il pesce si adagia sul fondo.
• Chiusura delle pinne.
• L’inefficienza del filtro può portare ulteriore stress alle koi con intossicazione da ammoniaca o nitriti.
• Morte della/e koi.Le ragioni di un aumento stabile oltresoglia del pH sono dovute ad introduzione di pesci troppo prematuramente in laghetti ancora non maturi, la dissoluzione di sostanze alcaline da rocce o dal cemento con cui è realizzato il laghetto, soprattutto se ancora fresco, eccesso di crescita di alghe o eccessiva piantumazione del laghetto.Le soluzioni a questo problema sono rappresentate da:
• Attendere la maturazione completa del laghetto stimolandola con aggiunta regolare di batteri al filtro.
• Diluizione degli alcali attraverso regolari cambi parziali di acqua.
• Rimuovere periodicamente l’eccesso di alghe.
• Usare composti acidificanti (operazione da fare sotto il controllo di una persona esperta).
Se il pH è troppo basso (pH<7,0: condizione definita acidosi) i sintomi sono questi:
• Bruciatura della pelle.
• Eccesso di produzione di muco (reattivo alla infiammazione).
• Il pesce boccheggia in superficie.
• Scoloramento o variazione dei colori della koi.
• L’inefficienza del filtro può portare ulteriore stress alle koi, con intossicazione da ammoniaca o nitriti.
• Stentata crescita di piante come il giacinto d’acqua, lattuga, elodea (piante normalmente a crescita infestante) e loro scoloramento.
• Morte della/e koi.Le cause di questa condizione sono imputabili a piogge torrenziali o a contenuto alto di sostanze acide (maggiormente presenti vicino a centri urbani o grandi città), scarsa riserva alcalina dell’acqua (basso KH), produzioni di sostanze umiche provenienti dalla decomposizione di foglie caduche.
SOLUZIONI
Le soluzioni a questo problema sono rappresentate da:
• Diluizione degli acidi attraverso regolari cambi parziali di acqua.
• Aggiungere Carbonato di calcio e gusci di ostriche per riequilibrare la riserva alcalina.
• Aggiungere sale all’acqua.


